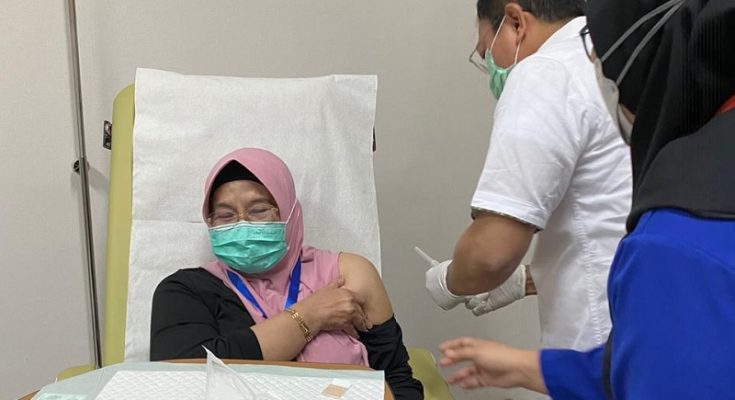
JAKARTA, AKSIKATA.COM – Badan Kesehatan Dunia (WHO) meliris jurnal terkait Vaksin Nusantara gagasan dr Terawan Agus Putranto di situs resminya, clinicaltrials.gov, pada Jumat (20/8).
Jurnal yang diberi judul “Preventive Dendritic Cell Vaccine, AV-COVID-19, in Subjects Not Actively Infected With COVID-19” itu mengulas uji vaksin dari dendritik sel itu.
Dalam jurnal itu disebutkan, tahap kedua uji klinis double-blind untuk pengujian anti-SARS-CoV-2 COVID-19 vaksin (AV-COVID-19), dibuat menggunakan peralatan vaksinasi PT AIVITA Biomedika Indonesia untuk mencegah infeksi COVID-19.
“Produk ini merupakan vaksin pribadi spesifik subyek yang terdiri dari sel-sel dendritik autologus dan limfosit (dci) yang sebelumnya telah dierami dengan sejumlah protein sari-cov-2 (S-protein) yang terbukti aman dalam tahap 1 studi yang juga dilakukan di Indonesia,” tulis Jurnal itu dikutip Askara, Sabtu (21/8).
Dalam studi tahap 2 ini, keberhasilan uji klinis dinilai melalui respons sel-t-protein-spesifik yang ditingkatkan dengan membandingkan hasil sebelum dan setelah vaksinasi.
“Keselamatan dikonfirmasi melalui nilai laboratorium, pengamatan dan laporan pasien reguler,” ungkap jurnal itu.
Dalam studi tahap 2 ini, dosis tunggal vaksin AV-COVID-19 disuntikkan pada lengan (kiri atau kanan) untuk memfasilitasi pemeriksaan dan menghindari reaksi pasca-injeksi atau nyeri bahu lokal.
Penilaian pasca-injeksi dilakukan pada 1, 2, dan 4 minggu setelah vaksinasi, dengan tes keamanan di laboratorium yang dilakukan pada minggu 1 dan 4, dan hanya pada minggu 2 jika ada perubahan klinis yang signifikan pada skrining hingga minggu 1.
Pada setiap pemeriksaan, tempat suntikan dinilai, dan subjek diajukan tentang gejala, dan pada minggu 0 (dasar sebelum injeksi), 2 dan 4, darah dikeluarkan untuk pengujian imunogenicity.
Data reaksi di situs injeksi dan profil keselamatan diperoleh melalui telepon untuk subyek pada hari 1, 2, dan 3 setelah injeksi vaksin,” lanjut Jurnal itu.
Subyek yang disuntikkan kemudian ditanya secara khusus tentang reaksi injeksi lokal dan gejala-gejala yang mirip flu sistemik (demam, menggigil, nyeri otot, nyeri sendi) selama 7 hari setelah injeksi.
“Kejadian-kejadian buruk (AE) dikumpulkan selama 28 hari setelah injeksi. Evaluasi tes laboratorium untuk parameter keamanan klinis dilakukan pada skrining juga segera sebelum vaksinasi dan pada hari 7 dan 28 pasca-vaksinasi. Kejadian yang merugikan (SAE), kondisi medis baru-baru ini, dan peristiwa lainnya yang membutuhkan intervensi medis dicatat selama 2 bulan setelah vaksinasi,” tambahnya.
Terakhir disebutkan, perangkat pengaktifan vaksin dibuat oleh PT AIVITA Biomedika Indonesia. Semua vaksin dibuat di Indonesia di rumah sakit dan klinik.